
我院杨宝峰院士团队在心肌缺血再灌注损伤领域取得新进展,研究成果论文《the positive feedback loop of the nat10/mybbp1a/p53 axis promotes cardiomyocyte ferroptosis to exacerbate cardiac i/r injury》于2024年4月2日发表于《redox biology》(if: 11.4)。该研究首次发现并阐明nat10诱导心肌细胞铁死亡促进心脏i/r损伤的潜在分子机制,为缺血性心脏病的临床防治提供了新思路与治疗靶点。
心肌缺血再灌注损伤(ischemia reperfusion, i/r)是指缺血性心脏恢复血液灌注后心肌损伤进一步加重的现象,是心律失常、心脏功能障碍和心衰发生发展的诱因。心肌i/r损伤机制复杂,涉及多重信号通路,但临床仍缺乏针对性的防治策略。因此,揭示i/r损伤的新调控分子机制和发现关键药物防治靶标是本领域研究难点和热点。铁死亡是一种铁依赖性脂质过氧化物过度累积诱导的细胞死亡方式,是心脏i/r损伤发生的重要机制。n-乙酰转移酶10(nat10)是催化rna ac4c修饰的乙酰转移酶,与多种疾病的病理生理过程密切相关,但其与心肌细胞铁死亡和心脏i/r损伤作用和机制仍不清楚。
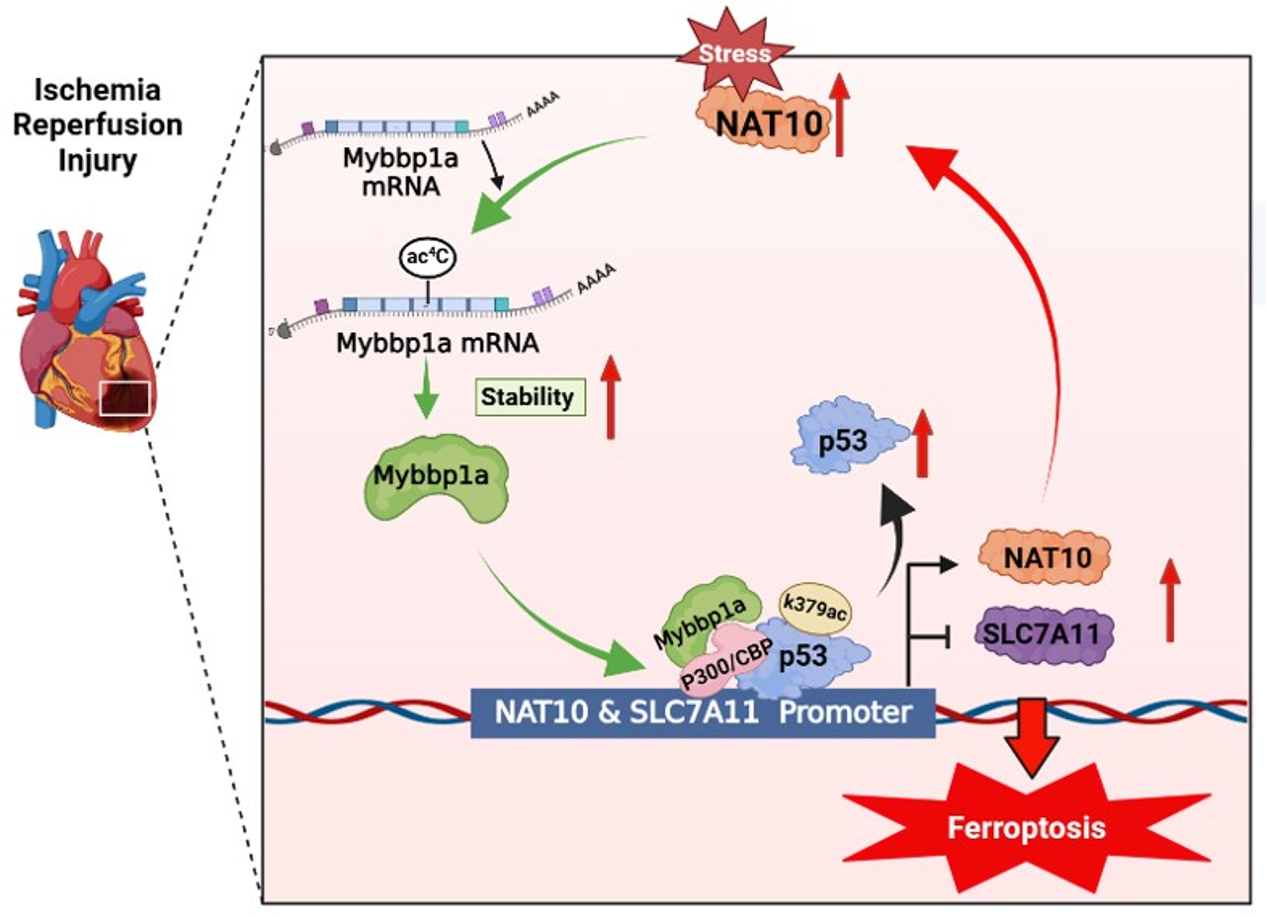
杨宝峰院士团队首次发现心脏i/r时表达上调的nat10通过介导mybbp1a mrna ac4c修饰增加其稳定性,进而促进p53乙酰化并增强其转录活性,降低铁死亡抑制因子slc7a11表达,从而诱导心肌细胞铁死亡加重心脏i/r损伤。反之,心肌细胞特异性敲除nat10或给予特异性抑制remodelin通过减轻心肌细胞铁死亡发挥心肌保护作用。进一步研究揭示p53作为转录激活因子促进nat10表达。该研究首次揭示了nat10/mybbp1a/p53正反馈环路在心脏i/r损伤的作用机制,为缺血性心脏病防治提供新策略。
我院杨宝峰院士、杜伟杰教授为本文共同通讯作者。曲哲哲博士、庞小琛硕士为本文共同第一作者。